Los péptidos recombinantes son terapias producidas a partir del método del ADN recombinante, una técnica que permite producir péptidos mucho más largos y complejos. La producción comienza con la fermentación utilizando un huésped microbiano, como el microorganismo bacteriano E. coli, o un microorganismo basado en la levadura, como S. cerevisiae o, más recientemente, la metilotrófica Pichia pastoris.
Estos microorganismos están diseñados para expresar el péptido recombinante de interés durante el proceso de fermentación. A diferencia del método sintético de producción de péptidos, el método recombinante produce una cantidad significativa de restos de células huésped, proteínas glicosiladas y otras impurezas que deben ser eliminadas después de la cosecha. Además, los péptidos recombinantes son propensos a la dimerización, agregación y fibrilación. Por lo tanto, el proceso de producción de recombinantes requiere múltiples pasos de procesamiento posterior -incluyendo varios pasos de cromatografía- para lograr la pureza deseada. No es raro que en la producción GMP se realice un paso de cromatografía de intercambio iónico (IEX) más uno o dos pasos de cromatografía de fase inversa (RPC).
El gel de sílice es el sustrato más comúnmente utilizado para la purificación de péptidos en fase inversa debido a su naturaleza robusta y a su probada capacidad de resolución; sin embargo, no todos los geles de sílice son iguales.
Purificación por cromatografía en fase inversa
Aquí nos centraremos en los pasos de la fase inversa. Existen varias consideraciones a la hora de seleccionar la fase estacionaria ideal para la purificación de péptidos recombinantes. El gel de sílice es el sustrato más común
utilizado para la purificación de péptidos en fase inversa debido a su naturaleza robusta y a su probada capacidad de resolución; sin embargo, no todos los geles de sílice son iguales. Un gel de sílice de fase inversa ideal debe contemplar
lo siguiente:
- Estabilidad alcalina: Dado que el material crudo está cargado con muchas impurezas diferentes, las columnas requerirán necesariamente una limpieza regular con agentes cáusticos entre ciclos. El CIP es un procedimiento muy utilizado para eliminar los péptidos autoagregados y fibrilados del lado de entrada del lecho de sílice de la columna. Este procedimiento de regeneración debe repetirse periódicamente para mantener la resolución, la separación de los picos y la baja contrapresión de la columna. Esto enfatiza la necesidad de un gel de sílice que sea químicamente compatible con condiciones alcalinas de hasta 0,1M de NaOH para la limpieza.
- Capacidad de enlace: Esta es una característica crítica para mejorar la economía de la separación. Con una mayor capacidad de carga, se puede purificar una mayor cantidad de péptido recombinante en cada ciclo.
- Robustez mecánica: En algunos casos, las columnas preparatorias o a escala de producción necesitarán
ser desempacadas y re-empacadas para mejorar la eficiencia de la columna y prolongar la vida útil del medio. Esto requiere un gel de sílice con una alta resistencia mecánica para soportar múltiples empaquetados de compresión axial.
Una nueva fase estacionaria diseñada para la purificación de péptidos complejos
Años de incesante trabajo de investigación y desarrollo en DAISOGEL condujeron al diseño y la fabricación de la fase estacionaria de base silícea más avanzada para resolver estos extraordinarios desafíos, a la que llamamos Serie PK.
Con un tamaño de partícula de 10 µm para una alta resolución y un tamaño de poro de 100 Å para una mayor capacidad de carga, también hemos desarrollado la serie PK con nuestra avanzada tecnología de modificación de la superficie, lo que da como resultado una inmejorable tolerancia al pH en comparación con otros geles de sílice de fase inversa del mercado. Además, su columna vertebral de sílice, especialmente diseñada y fabricada, proporciona una resistencia mecánica adicional a las partículas de sílice. Para probar las capacidades de PK Series en condiciones reales, realizamos un riguroso estudio de caso purificando una muestra de insulina cruda.
Más información en nuestro nuevo folleto PK
ESTUDIO DE CASO: Aplicación de la serie PK para lograr una pureza superior al 99% en la insulina cruda
En esta nota técnica demostraremos cómo la Serie PK fue capaz de llevar una alimentación de insulina cruda de sólo el 72,5% de pureza y elevar la pureza a más del 99%. La pureza inicial de la muestra cruda se verificó mediante un análisis de HPLC analítico, como se ve a continuación.
Como ya se ha visto, la baja calidad de la solución de alimentación bruta dificultó la modelización posterior. Se utilizó una etapa de cromatografía de intercambio catiónico fuerte basada en polímeros bien ejecutada (no mostrada) para elevar la pureza hasta el 88,0%. Para alcanzar la pureza final deseada, se emplearon dos etapas de RPC con PK Series.

RPC Paso 1: gradiente de ACN contra sulfato de amonio
ácido sulfúrico en la serie C8-PK
En el primer paso de RPC, se sobrecargó una columna DAISOGEL SP-100-10-C8-PK preparada con 15 g/L de insulina purificada con IEX. Con el objetivo de un rendimiento del 90%, se aplicó un gradiente de acetonitrilo sobre un fondo de sulfato de amonio/ácido sulfúrico en las condiciones que se muestran a continuación.
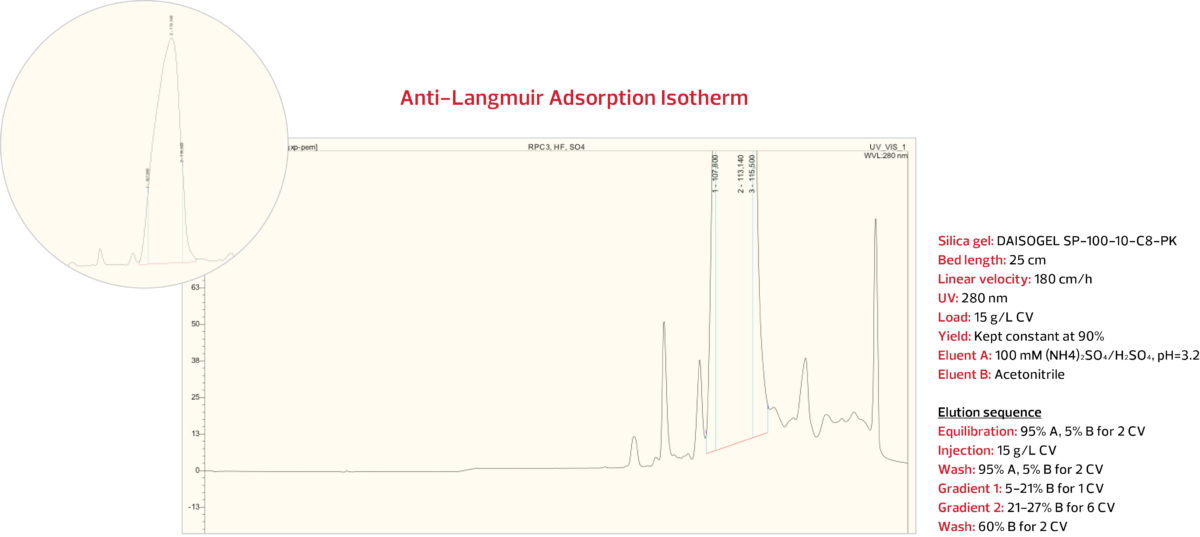
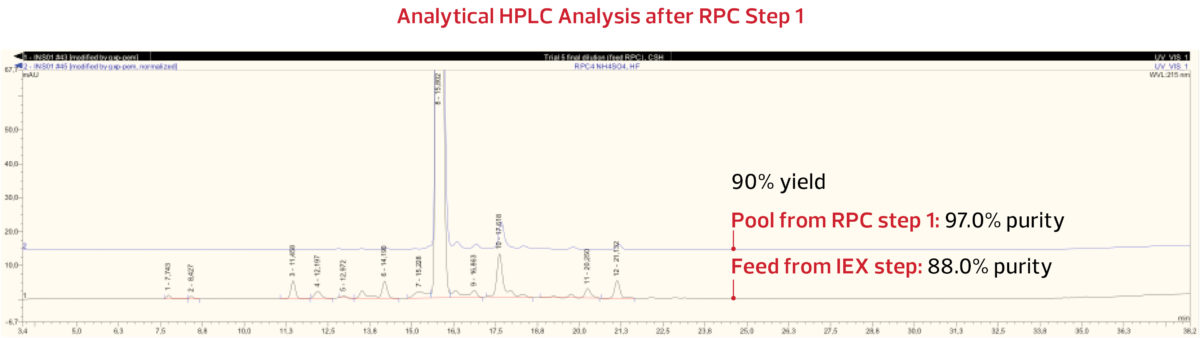
El pico de insulina se recogió y analizó. Los resultados analíticos de HPLC del pool RPC Paso 1 indican
que con un rendimiento del 90% se obtuvo una pureza del 97,0%, como se muestra a continuación.
RPC Paso 2: gradiente de ACN contra acetato de amonio
ácido acético en la serie C8-PK
Para lograr la pureza deseada de >99,0%, se empleó un segundo paso de RPC. Se sobrecargó una columna DAISOGEL SP-100-10-C8-PK con 15 g/L de insulina purificada con RPC1. Con el mismo objetivo de 90% de rendimiento, se aplicó un gradiente de acetonitrilo, pero esta vez contra un fondo de acetato de amonio / ácido acético, bajo las condiciones que se muestran a continuación.
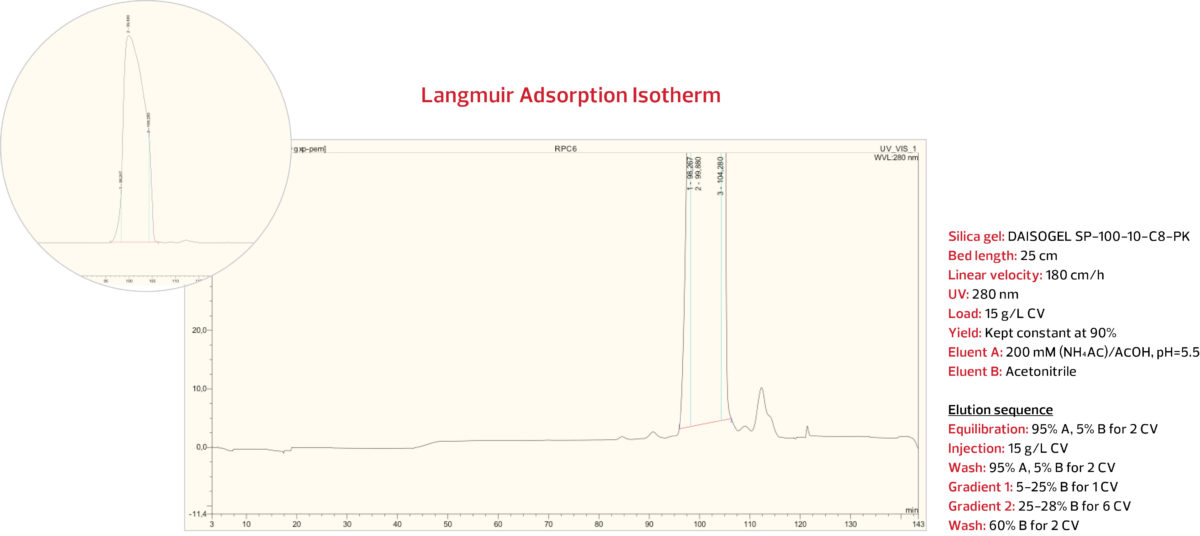
DAISOGEL SP-100-10-C8-PK
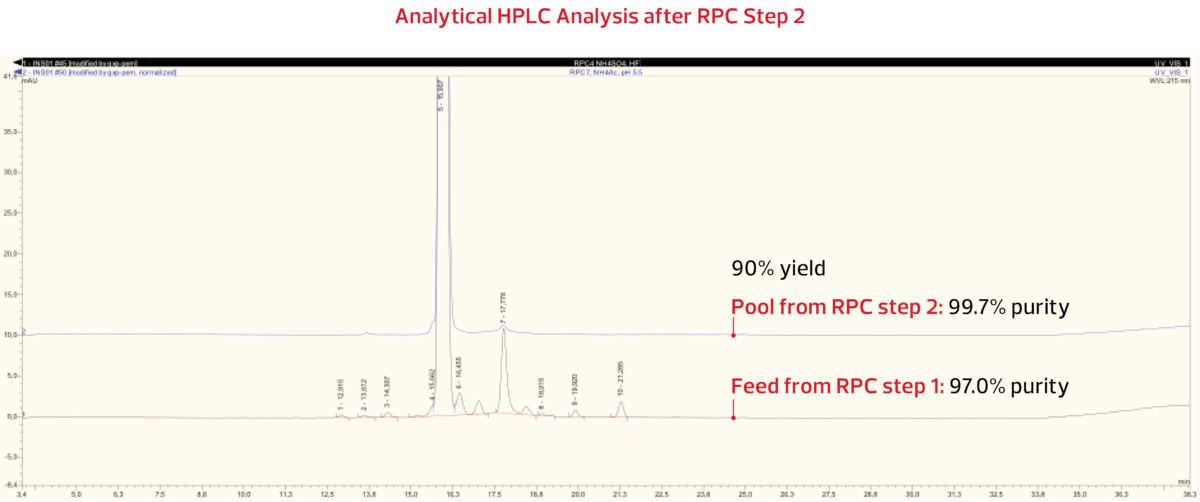
El pico de insulina se recogió de nuevo y se analizó. Los resultados analíticos de HPLC del pool de RPC Paso 2 indican que con un rendimiento del 90%, se obtuvo con éxito una pureza del 99,7%, como se muestra a continuación.
Conclusión
Los péptidos recombinantes son complejos por naturaleza y difíciles de purificar, siendo la insulina un ejemplo clásico. Llevar la pureza de estos compuestos a más del 99% sin sacrificar el rendimiento es importante tanto por la seguridad del producto como por razones económicas. Se seleccionó el gel de sílice DAISOGEL de la serie C8-PK para purificar un material de insulina crudo de baja pureza debido a su elevada área superficial, capacidad de carga, resistencia mecánica y poder de resolución.
Al emplear una purificación RPC de dos pasos después de un paso IEX, pudimos lograr con éxito una pureza del 99,7% sin sacrificar el rendimiento.
| Paso | % de pureza |
|---|---|
| Pienso en bruto | 72.5 |
| IEX | 88.0 |
| RPC1 | 97.0 |
| RPC2 | 99.7 |
